Фото Scott Beckner (flickr.com/piratescott)


Борис Штерн Михаил Никитин
Беседа главного редактора ТрВ-Наука Бориса Штерна с биологом Михаилом Никитиным о возможных альтернативных вариантах происхождения, эволюции и распространении жизни. Видеозапись интервью — youtu.be/meZIL_AzXx8. См. предыдущие публикации: trv-science.ru/tag/proisxozhdenie-zhizni.
— Добрый день! Сегодня у нас на канале «Троицкого варианта» опять, опять, в который раз Михаил Никитин и наверняка не в последний раз. И сегодня мы будем говорить об альтернативных формах жизни. Потому что когда начинаешь рассуждать о вероятности возникновения жизни на Земле, о пригодности планеты для жизни, сразу начинаются возражения: «Вы говорите о нашей жизни, а жизнь может быть любой. То есть она может существовать совершенно в других условиях, которые вы представить себе не можете…»
И вот давайте попробуем себе представить эти другие формы жизни, другие условия, в которых она может существовать. И попробуем начать, наверное, с самой популярной идеи: возьмем-ка мы вместо углерода кремний и попробуем построить жизнь на основе кремния. У нас, дескать, получится что-нибудь совсем другое, интересное. Что думаете по этому поводу, Михаил?
— Я думаю, что тут надо разобраться: а что конкретно надо строить из кремния? Если попытаться из кремния построить точные аналоги наших белков и нуклеиновых кислот, то это не получится. Химия кремния и химия углерода все-таки не настолько похожи. Поэтому стоит сначала разобраться с какими-то более общими особенностями того, что мы считаем жизнью. Как и везде в естественных науках, в отличие от математики и философии, мы тут не можем начать с того, чтобы дать строгое определение, что такое жизнь. Но пока мы находимся на Земле и рассматриваем то, что есть на Земле, мы более-менее интуитивно понимаем, что там живое, а что не живое. То есть царства растений, животных и минералов люди выделяли тысячи лет назад.
Некоторую сложность доставляли вирусы, но тут я могу сказать, что вирусы, конечно же, живые, хотя бы потому, что кафедра вирусологии находится на биологическом факультете, а не на химическом и не на геологическом. Вирусы способны к размножению, также, как и все другие живые существа, просто те формы вирусной частицы, которые кристаллизуются и более упорядочены, чем живые клетки, — это их покоящаяся стадия. А активная форма жизни вируса — это вироклетка, зараженная клетка, которая производит новые вирусные частицы. Она со всей очевидностью живая — это размножающаяся форма живого организма, вируса.
Структура свернутого белка. «Википедия»
Значит, всё живое на Земле — и клеточные, и вирусные формы жизни — построено на одних и тех же химических соединениях, на двух основных классах полимеров — это белки и нуклеиновые кислоты, т. е. ДНК и РНК. Полимеры — это молекулы в виде длинных линейных цепочек, состоящих из нескольких типов повторяющихся звеньев. Те полимеры, что более привычны химикам, — такие, как полиэтилен, полистирол, — состоят из одного типа звеньев. Биополимеры — из нескольких типов звеньев, т. е. в белках — двадцать возможных вариантов аминокислот, в ДНК и РНК — четыре возможных варианта нуклеотидов. И последовательность этих разных звеньев в нуклеиновых кислотах используется для кодирования информации. На этом сходство между белками и нуклеиновыми кислотами, в общем, заканчивается. Важно то, что они совершенно по-разному сворачиваются в трехмерные структуры. И белок, и ДНК можно вытянуть в прямую цепочку, но в естественных условиях в водном растворе ни тот, ни другой не будут принимать форму прямой цепочки. Для ДНК наиболее стабильная форма — это двойная спираль из двух антипараллельных нитей. Ну и вот спираль будет уже более-менее прямой. А белки, как правило, сворачиваются в сложные трехмерные клубки. И это определяется их физико-химическими свойствами. У молекул нуклеиновых кислот есть размазанный по всей их длине электрический заряд, они же кислоты, т. е. в водном растворе заряжены отрицательно, и кулоновское отталкивание разных частей цепочки ДНК друг от друга не позволяет ей свернуться в клубки. А у белков нет глобального электрического заряда —наоборот, белковая цепочка и ее пептидные связи представляют из себя цепочку диполей, которые способны довольно эффективно и специфически друг к другу притягиваться. И взаимодействие этих диполей обеспечивает сворачивание белков в базовые трехмерные формы альфа-спирали или бета-складчатого слоя и дальше в более сложные уже третичные пространственные структуры, в сложные клубки, которые необходимы для работы этих белков в живом организме. И белки, и нуклеиновые кислоты, построенные из атомов (в первую очередь углерода), и прочные связи С–С (углерод-углеродные) играют основную роль в их стабильности.
Кроме того, разрыв этих цепочек — как случайный, какими-то внешними факторами, так и целенаправленный — ферментами, протеазами и нуклеазами — происходит не где попало, а по границам между звеньями, между мономерами, как если бы мы конструкцию из блоков LEGO стали растягивать, — она бы разломалась на отдельные целые кубики, из которых можно собрать какую-то новую, другую конструкцию. То есть мономеры не ломаются так просто, как связи между ними. Связи между мономерами более слабые, чем внутри мономера. Более слабые связи между мономерами обеспечиваются не углеродом, а другими химическими элементами — азотом в белках и фосфором в нуклеиновых кислотах.
Вот это вот повторное использование «кирпичиков» после распада целого белка или целой молекулы нуклеиновой кислоты — тоже важная часть их жизненного цикла внутри живых организмов. Насколько мы можем судить, для жизни нужны полимерные молекулы, способные сворачиваться в трехмерные структуры, как белки, потому что это нужно для важнейшей функции большинства белков — для катализа. Большинство белков — это ферменты, т. е. ускорители определенных химических реакций, специфичные ускорители. Белковый катализ гораздо более специфичен, чем катализ разными малыми молекулами, комплексами металлов и т. д. Специфичность достигается за счет того, что белковый клубок — белковая молекула — имеет «карманы» для реагирующих внутри нее маленьких молекул определенной формы, которые позволяют им подойти друг к другу только определенной стороной и никакой другой, а заодно изолируют их от других молекул, норовящих вмешаться в эту химическую реакцию, — в том числе, как ни странно, и от воды, от которой во многих случаях биохимические реакции приходится «прятать» внутри фермента.
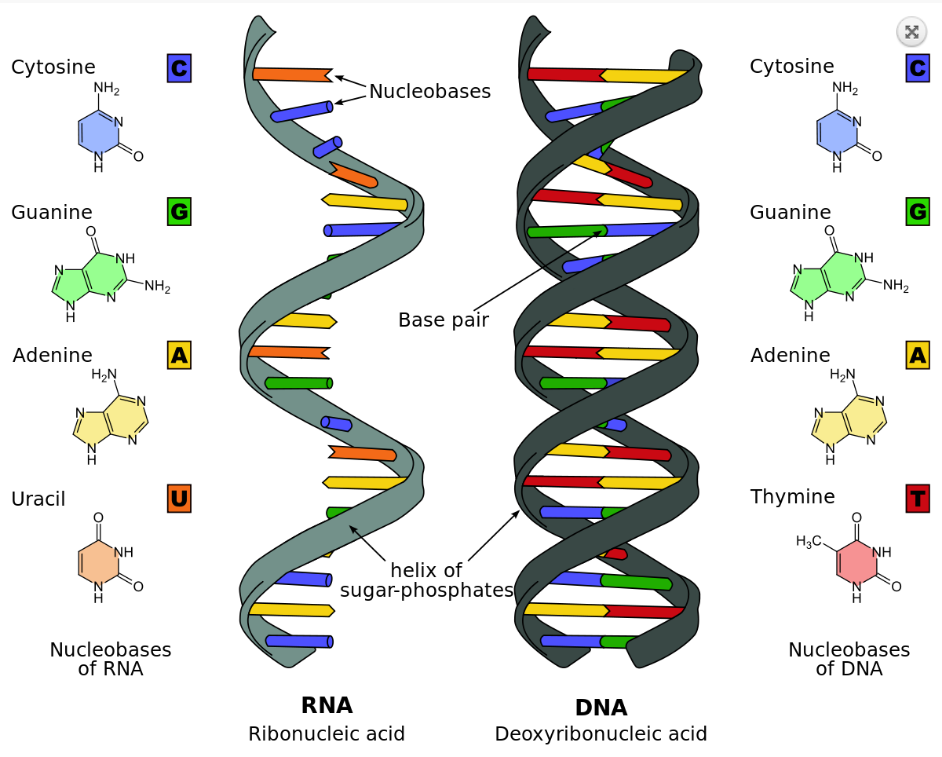
Нуклеиновые кислоты кодируют своей последовательностью последовательность белков. Нуклеиновые кислоты несут функцию памяти в биологической системе. В принципе, возможно совместить и функцию памяти, и функцию катализа в одном биополимере. На заре земной жизни и на этапе мира РНК предположительно так и было, но это гораздо менее эффективно. РНК — менее надежный носитель информации, чем ДНК, и РНК гораздо более ограничена как катализатор по сравнению с белками. Поэтому мир РНК существовал, скорее всего, очень недолго и быстро уступил место более сложным организмам, использующим также и белки. Но, в принципе, жизнь на одном полимере, так прямо с порога отметать нельзя.
Можно ли представить себе жизнь, вообще не использующую полимерные молекулы, на основе растворимых мономеров, или на основе трехмерных кристаллов, или на каких-то нехимических структурах типа плазмоидов? (Про плазмоиды я сразу скажу честно, я ничего про это не знаю. И реальность такой жизни оставим оценивать тем специалистам — видимо, физикам, — которые лучше в этом понимают.) А вот про кристаллы и растворы малых молекул у меня есть, что сказать, в частности, почему они считаются не очень хорошей основой для жизни. Потому что жизнь довольно четко отличается от неживой материи на Земле по способности к дарвиновской эволюции, по способности к неограниченной наследуемой изменчивости. Так, живые организмы производят свои копии, копии эти не являются точными — они все-таки немножко отличаются от родителей, — изменения этих копий наследуются следующими поколениями (это не одна ошибка, которая будет исправлена в следующем поколении, это наследуемое изменение), а разница между этими копиями влияет на их дальнейшее размножение. Существует отбор. Какие-то потомки с какими-то вариациями размножаются лучше, другие потомки с другими вариациями размножаются хуже и в конце концов могут исчезнуть из популяции.
Дарвиновский естественный отбор — это очень важный процесс. Более того, он входит в рабочее определение астробиологической программы NASA. Там определение очень короткое: «Жизнь — это химическая система, способная к дарвиновской эволюции». Но какой должен быть материальный субстрат, чтобы поддерживать дарвиновскую эволюцию? Он, строго говоря, не обязан быть химическим. Есть такое направление в computer science — эволюционное программирование, когда механизм дарвиновской эволюции прилагается к фрагментам программного кода и позволяет получить таким способом программы, выполняющие какую-то нужную функцию. При этом никакой химии там нет. Там нет молекул и атомов, там есть нули и единицы — электрические сигналы. Но маловероятно, что мы найдем что-то подобное дарвиновскому отбору электрических сигналов в природе, потому что это все-таки работает на компьютерах, созданных разумными существами. Очень трудно себе представить обнаружение в природе естественно возникших электронных компьютеров, причем возникших без участия дарвиновской эволюции — в каком-то готовом виде.

Эрвин Шрёдингер. Что такое жизнь с точки зрения физики?
А что же с химическими носителями? Во-первых, почему растворы малых молекул не могут быть базой для дарвиновской эволюции? Потому что они не являются надежным носителем химической информации. Концентрацией разных веществ в растворе можно закодировать довольно много информации, но это будет ее аналоговая запись — концентрации молекул можно менять плавно. А вот изменение последовательности полимера (замена аденина на гуанин в ДНК, условно говоря) — это дискретное изменение, которое может происходить только при преодолении какого-то энергетического барьера. А поскольку спектр тепловых шумов устроен так, что вероятность сильных фуктуаций гораздо меньше, чем слабых, а слабые флуктуации, способные повредить концентрационный геном (изменить концентрацию молекул в растворе), они гораздо-гораздо более вероятны. И первым подошел к осознанию этих вещей еще Эрвин Шрёдингер в знаменитой своей брошюре «Что такое жизнь с точки зрения физика?». Эта брошюра, кстати, подсказала Уотсону и Крику, что надо искать, как должен выглядеть носитель наследственной информации. Дальнейшими работами было строго доказано, что дарвиновская эволюция возможна только при цифровой записи наследственной информации: аналоговая запись не работает. Аналоговая запись наследственной информации будет неизбежно разрушена мутациями, случайными тепловыми шумами быстрее, чем естественный отбор сможет ее стабилизировать или улучшить. Таким образом, растворы малых молекул в качестве живой материи не очень подходят.
У кристаллов же всё хорошо со стабильностью, но для трехмерных кристаллов гораздо сложнее придумать какой-то разумный, простой механизм копирования, который имеется у одномерных линейных полимеров. В принципе, можно себе представить для каких-нибудь искусственных организмов механизм записи наследственной информации двумерный, по аналогии с QR-кодом, но понятно, что система его чтения и копирования будет гораздо сложнее, чем существующие природные ДНК-полимеразы, которые копируют одну нить на другую, используя свойства комплементарного соединения азотистых оснований. Собственно, из двуспиральной структуры ДНК-РНК механизм их репликации — копирования — следует довольно простой и очевидный. То, что Уотсон и Крик предсказали этот механизм репликации, даже важнее, чем то, что они расшифровали двуспиральную структуру.
Итак, растворы малых молекул без полимеров слишком уязвимы к мутациям, а кристаллы, наоборот, очень стабильны и неудобны для копирования. Одномерный носитель — линейный полимер, — похоже, является таким оптимумом. И при поиске жизни на альтернативной химической основе нам все-таки надо ориентироваться на линейные полимеры.
А теперь: какие химические элементы вместо преобладающего в нашей жизни углерода можно рассмотреть? Научные фантасты вот очень любили кремний. Он находится в таблице Менделеева под углеродом, тоже имеет валентность 4, широко распространен в природе, более того, на Земле его даже гораздо больше, чем углерода. Но у меня большие сомнения в возможности существования кремниевой жизни где-то в природе. И вот почему. Хотя на основе кремния, созданном химиками, есть множество Кремнийорганических соединений, содержащих цепочки и кольца из атомов кремния (в том числе с включением углерода, азота, серы и других гетероатомов), для синтеза почти всех этих сложных химических соединений кремния нужны безводные среды. В присутствии воды и в присутствии кислорода наиболее устойчивая, с большим отрывом, термодинамически устойчивая форма кремния — это оксиды кремния и силикаты. Это те горные породы, которые мы видим вокруг себя на Земле: как в природе, так и в городе в виде всякого гравия в составе бетона. Соединения кремния с кислородом очень прочные, очень стабильные. Это трехмерные кристаллы. Более того, не только на Земле, но и в метеоритах и даже в наблюдаемых методами радиоастрономии туманностях кремний существует в основном именно в этой форме. Для углерода радиоастрономы нашли более сотни органических молекул в межзвездной среде, в том числе таких достаточно сложных, как глицин, этанол и уксусная кислота, а вот для кремния аналогичным образом обнаруживаются в основном простые двухатомные молекулы, соединения кремния с углеродом, с кислородом, с азотом, с серой и т. д., которые при повышении концентрации будут образовывать устойчивые кристаллы — карбид кремния, нитрид кремния, оксид кремния. Прочные тугоплавкие соединения.
А можно ли избежать кислорода и воды в нашей Вселенной? Это очень-очень сложно, потому что кислород — третий по распространенности элемент во Вселенной после водорода и гелия. И вода, образуемая первым по распространенности водородом и третьим по распространенности кислородом, тоже есть в космосе практически везде. В лаборатории можно, в принципе, наверное, организовать какую-то безводную среду и искусственную жизнь на кремнийорганических полимерах, но естественную нишу, где не будет воды, не будет кислорода и каких-то других активных кислородосодержащих соединений вроде диоксида углерода СО2, — уже сложно. Ну и при сверхнизких температурах, когда вода и кислород вымораживаются, прочность связей кремния и кислорода будет такая, что эти связи будут существовать вечно. Пустить оксиды кремния в какую-то химическую реакцию, в какой-то обмен веществ будет невозможно. Получается, кремний подводит его слишком большая «любовь» к кислороду. Связь кремний-кислород слишком прочна, прочнее, чем все связи, образуемые углеродом с другими атомами, и практически нет реального способа вовлечь эти связи в какие-то химические реакции в мягких условиях.
— Ну, например, стекло и кварц…
— Верно. Чтобы химически во что-то превратить стекло или кварц, нужны либо температуры выше 1000 °C, либо такие жесткие реагенты, как плавиковая кислота (HF), либо обработка концентрированными щелочами. И то, и другое, и третье очень плохо совместимо с существованием каких-то сложных молекул, необходимых для жизни. Химические свойства кремния на самом деле довольно сильно отличаются от химических свойств углерода. И тут мы ничего хорошего для потенциально альтернативной биохимии найти не можем. Мы уже упомянули другой альтернативный химический элемент — это фтор. Его соединение с водородом, плавиковая кислота — это хороший полярный растворитель, который кое-где в фантастике встречался как замена воды. Например, у Ефремова была фтороводородная жизнь. Но фтор подводит ядерная физика. Единственный стабильный изотоп фтора — фтор-19 — довольно мало распространен во Вселенной, плохо образуется в термоядерных реакциях в звездах, и в результате фтора во Вселенной в миллион раз меньше, чем кислорода.
И химические свойства фтора не настолько уникальны, чтобы он где-то так хорошо сконцентрировался, чтобы в нашей или в другой галактике была где-то планета с фтороводородным океаном. Насколько мы можем судить, ядерная физика работает одинаково во всей видимой Вселенной, поэтому фтор в дефиците будет везде. На Земле это достаточно редкий микроэлемент, который большинство живых организмов никак особо не используют. Исключение — это только мы с вами, позвоночные животные, которые фторидом кальция упрочняют свои зубы. Поэтому для нас лично фтор важен, а вот для большинства земных организмов он не требуется совершенно.
Что еще из интересных химических элементов? Бор — это элемент с интересной разнообразной химией, которая в последние годы как раз активно изучается. Бор находится в соседней с углеродом колонке таблицы Менделеева. У него основная валентность 3. Но в соединениях с азотом он может имитировать валентность 4 за счет донорно-акцепторных связей. И, чередуя атомы бора и азота, можно имитировать углеродную органику. Например, есть боразол — неорганический аналог бензола. А на основе бора без азота образуются свои интересные химические достаточно активные соединения с интересными структурами. Таким образом, жизнь на основе бора в лаборатории, наверное, можно сделать. А вот в природе бор так же, как и фтор, подводит ядерная физика. У него тоже не очень стабильное ядро, поэтому в условиях нуклеосинтеза в звездах бор не образуется, а наоборот, быстро превращается в более тяжелые элементы. И тот бор, который есть у нас на Земле и в межзвездном пространстве, образуется, насколько я помню, в основном в реакциях космических лучей с межзвездной материей. И это гораздо менее эффективно, чем нуклеосинтез в звездах. Естественную жизнь на основе бора мы тоже вряд ли найдем где-то во Вселенной. И вообще, если посмотреть на график распространенности химических элементов, можно увидеть, что наша земная жизнь выбрала самые распространенные: из первой десятки самых распространенных химических элементов — водород, гелий, кислород, углерод, азот, сера, магний, кремний, железо и неон, — она использует семь. Не попали только инертные газы — гелий, неон — и тот самый кремний, который не газ, но в соединениях с кислородом тоже химически инертен. А так и магний имеет важные функции в земной жизни (нуклеиновые кислоты и нуклеотиды всегда в растворе находятся вместе с ионами магния), и сера имеет важную роль в биохимии, и железо… Наша земная биохимия на самом деле довольно хорошо подогнана под доступность химических элементов во Вселенной, определяемую ядерной физикой. И альтернативную биохимию, альтернативную земной, надо искать, видимо, в пределах тех же самых химических элементов: кислорода, углерода, азота, серы, железа и т. д.
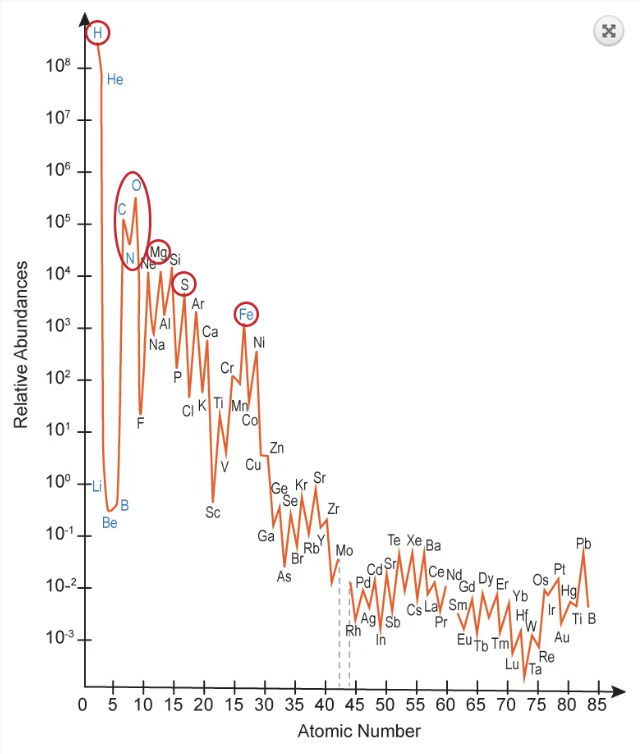
Рис. 1. Земная жизнь использует семь из топ-10 самых распространенных элементов — водород, углерод, кислород, азот, сера, магний, железо
Земная жизнь использует семь из топ-10 самых распространенных элементов — водород, углерод, кислород, азот, сера, магний, железо (trv-science.ru/2023/06/panspermiya-i-alternativnaya-bioximiya/)
Есть ли тут простор для фантазии? На самом деле есть. Только, насколько мне известно (пусть поправят меня любители фантастики), писатели-фантасты в эту сторону смотрели меньше. А так тут есть варианты. И больше всего мне нравится идея про замену воды на сжиженный диоксид углерода СО2 под давлением. Диоксид углерода в наших обычных земных условиях — это либо газ, либо твердое вещество, сухой лед. При нашем атмосферном давлении он не сжижается, но если повысить атмосферное давление, то он превращается в жидкость, причем является очень хорошим растворителем. Жидкий диоксид углерода под давлением растворяет как полярные вещества, так и неполярные; как органические, так и неорганические. Он уже используется в промышленности как достаточно дешевый экологически чистый растворитель. Вот, например, бескофеиновый кофе делают с его помощью, экстрагируя кофеин с жидким СО2. Более того, в химической технологии используются наши обычные белковые ферменты из земных бактерий, работающие в среде жидкого СО2. Такая среда позволяет им эффективно и быстро работать с неполярными молекулами, такими как жиры. За счет этого в среде жидкого СО2 белковые ферменты, отобранные на работу в воде, работают в сотни раз быстрее, чем в воде. А ведь можно было бы ожидать, что в родном растворителе, для которых их оптимизировал естественный отбор, они должны работать лучше. Но жидкий СО2 отличается малой вязкостью по сравнению с водой, в нем быстрее диффузия молекул, поэтому вход субстратов, фермент и выход продукта происходит быстрее.
Более того, на Земле есть места, где жидкий СО2 лежит просто небольшими озерами. Это некоторые гидротермальные районы на морском дне. Наиболее изученные — те, что находятся на глубине около полутора километров в Окинавском желобе у берегов Тихого океана. Благодаря работам японских океанологов мы знаем, что там рядом с горячими источниками, черными курильщиками, есть высачивание холодного жидкого СО2 — жидкого за счет высокого давления, существующего на этой глубине. Он образует озера, скрытые под тонким слоем глины, под океанским дном. Подводные роботы брали пробы из этого углекислотного озера, расковыривая глинистую корку, и обнаружили, что в этой среде, в этом альтернативном растворителе, живут микробы. Обычные земные микробы, более-менее те же виды, что встречаются в некоторых других местах на морском дне, на большой глубине, только они имеют слегка модифицированный состав клеточных мембран, потому что стандартные липидные мембраны жидкие СО2 все-таки растворяют. Но небольшого изменения мембран оказывается достаточно, чтобы приспособить земную жизнь к этому альтернативному растворителю. В нем работают белки, внеклеточные белки этих микробов, в общем, такие же, как у их родственников, живущих в воде. Главное неизвестное тут: можно ли приспособить к такому растворителю ДНК, нуклеиновые кислоты? У этих микробов все-таки внутри клетки среда водная, а не углекислотная. Они поддерживают внутри клетки привычную водную среду. Но как минимум белки можно к этому приспособить, к этому альтернативному растворителю. И — да поправят меня астрономы, — но насколько я понимаю, океаны из жидкого СО2 можно ожидать на каких-нибудь планетах более холодных и массивных, чем Земля, на каких-то холодных суперземлях.
— Если жидкий СО2, то вот сразу вопрос о жидком метане в качестве растворителя — потому что он есть, мы его наблюдаем в Солнечной системе.
— Да, жидкий метан мы наблюдаем на Титане, на спутнике Сатурна, но тут как раз химики настроены более скептично. Если жидкий СО2 — это диапазон температуры относительно близкий к комнатному (ну, до –33 °C), то вот жидкий метан — это уже криогенные температуры порядка минус 170–180 °C. И если в молекуле СО2 есть полярные связи, хотя нет глобального дипольного момента, то молекула метана неполярна совсем. Поэтому жидкий метан является довольно плохим растворителем. В нем растворяются только маленькие и неполярные молекулы, а больших массивных полимеров масштаба белков и нуклеиновых кислот растворить в жидком метане не получится. Ионы металлов в нем тоже не растворяются. Химия в жидком метане из-за того, что это очень плохой и очень выборочный растворитель, получается очень бедной.
Жидкий аммиак выглядит лучше. Жидкий аммиак полярен подобно воде, но мы нигде не наблюдаем жидкого аммиака в чистом виде. Насколько я помню, в Солнечной системе везде, где есть аммиак в большом количестве, к нему примешано еще больше воды, точно?
— Ну, это планета-гигант, и, в принципе, там жидкий аммиак мог бы быть. Ну, какой-нибудь там Нептун…
— То есть в ледяных гигантах и на спутниках планет-гигантов аммиак всегда примешан к воде, да?
— Видимо, да.
— Даже водная аммиачная смесь, концентрированный нашатырный спирт, в принципе, могла бы быть растворителем для альтернативной биохимии, потому что это сильно щелочная среда. Все земные организмы поддерживают внутри клетки более-менее нейтральную среду pH от 6 до 8, независимо от того, в какой среде они живут — хоть в страшно кислой, хоть в крайне щелочной. И это важно, потому что уотсон-криковские пары между азотистыми основаниями ДНК образуется только в нейтральной среде. И в кислой, и в щелочной среде ДНК перестает выполнять функцию генетического полимера. Поэтому в водно-аммиачной среде химия и полимеры на углеродной основе возможны, разнообразны, но нуклеиновые кислоты понадобится заменять какими-то другими полимерами, которые могут тоже, наверное, образовывать двойную спираль. К форме двойной спирали претензий нет, но вот химическая реализация для водно-аммиачной среды, конечно, должна быть другой. А вот белки там, в принципе, могут использоваться.
— Вопрос вдогонку. Пусть будет углеродная жизнь — углеродно-водная, — но где-нибудь в очень необычной среде, например под толстым слоем льда и воды на тех же спутниках ледяных планет-гигантов — Европе, Титане, Энцеладе. Там, судя по всему, очень щелочная среда. Света там нет, но какая-то химия там есть. Там, наверное, тоже может быть жизнь…
— Смотрите, на Земле микробы существуют в довольно экстремальных средах. Они присутствуют в вечной мерзлоте и в горячих источниках при температурах почти до 120 °C при высоких давлениях. Кроме того, микробы обнаруживаются в толще земной коры на глубинах до 4–5 км, и их распространение вглубь ограничивается только уже повышением температуры с глубиной. То есть микробных экосистем в экстремальных условиях известно довольно много. В изолированных от света микробных экосистемах они питаются при помощи хемосинтеза, используя в качестве пищи углекислый газ, соединения серы, молекулярный водород и т. д. Могут использовать и, например, окислительно-восстановительные реакции между металлами. По минимуму достаточно, чтобы был углекислый газ и водород. Микробы могут получать энергию, синтезируя метан из этих двух исходных веществ, и такой метаногенный метаболизм встречается на самых больших глубинах в земной коре, где еще температуры не превышают сотни градусов. И земные микробы-экстремофилы, в принципе, могли бы жить и в подледных океанах спутников планет-гигантов, таких как Европа и Энцелад. Околонулевые температуры, темнота, высокое давление — всё это им нипочем. Какие тут неизвестные факторы? Во-первых, мы не знаем, достаточно ли там постоянных высачиваний водорода и углекислого газа из недр этих спутников. Во-вторых, мы не знаем, достаточно ли там переходных металлов, микроэлементов, которые необходимы этим микробам. То есть углекислый газ и водород — это источники энергии, как нам углеводы и жиры, а вот микроэлементы все-таки нужны отдельно, даже микробам. И фосфор нужен. Что с доступностью этих элементов в подледных океанах, мне неизвестно и неизвестно никому, потому что зонды туда еще не проникали под лед. Да?
— Да. Там, судя по всему, подводный вулканизм развит, во всяком случае, на Европе, потому что соседний спутник — Ио — жутко вулканический. От того, что его плющат приливные силы из-за эллиптичности орбиты. Европу тоже плющит, только в меньшей степени…
— На Европе из-за приливного разогрева мы можем ожидать гидротермальной активности и подводных вулканов. Это обнадеживает в плане доступности металлов, но с фосфором не всё так просто. На Земле весь фосфор, который поступает в океаны, оказывается там в результате эрозии суши, в результате разрушения горных пород выше уровня моря. Поэтому и под ледяной корой, и на незамерзшей планете-океане, где суши нет, а есть глобальный океан, можно предполагать проблемы с биологической доступностью фосфора. Потому что под водой выветривание горных пород не работает так хорошо, как на суше. Конечно, это только предположения, но их как-то надо проверять космическими зондами или дистанционным исследованием экзопланет. Дефицит фосфора может довольно сильно ограничить продуктивность микробной биосферы…
— В атмосфере планет-гигантов довольно сложная химия. Можно там придумать что-нибудь интересное с точки зрения жизни?
— С точки зрения жизни, мне кажется, там всё упирается в проблему, как для более-менее крупных частиц избежать падения вниз, в зону высоких температур.
— Допустим, конвекция поддерживает восходящие потоки. Ну, болтаются вверх-вниз…
— Тогда протоклетка должна, как орел, парить на восходящих потоках. Да, болтаются. Это требует от нее с самого начала довольно сложной координации движений. Боюсь, это нереально.
— Это естественный отбор: те, которые не падают, выживают.
— Если сначала упадут все, то отбор будет не из кого проводить. Тут смотрят, наверное, на ледяные гиганты, и особенно на экзопланетные ледяные гиганты, которые есть еще поменьше Урана и Нептуна и у которых температура с глубиной нарастает не так быстро. И тут можно вспомнить, кстати, о работах Артёма Оганова по моделированию соединений азота и водорода при сверхвысоких давлениях, существующих в центрах ледяных гигантов. В этих условиях азот может образовывать сложные трехмерные структуры, цепочки и кольца подобно углероду. При нашем обычном давлении он это всё не образует, но при высоких давлениях они стабилизируются, и, наверное, какая-то жизнь на азотной основе внутри ледяных гигантов может быть. Правда, у этой жизни будет очень незавидная судьба — она никогда не сможет выйти в космос. При попытке покинуть свою колыбель высокого давления она просто взорвется, превратившись в газообразный азот.
— Ну, в принципе, так сказать, пофантазировать на эту тему можно…
— Пофантазировать можно, но вот вступать в контакт с такой жизнью будет очень сложно, даже если она разумна.
— Есть ли какие-нибудь еще возможные неожиданные варианты для обитания жизни? Они вообще кем-то обсуждались? Вот вам в голову сейчас ничего не придет по этому поводу?
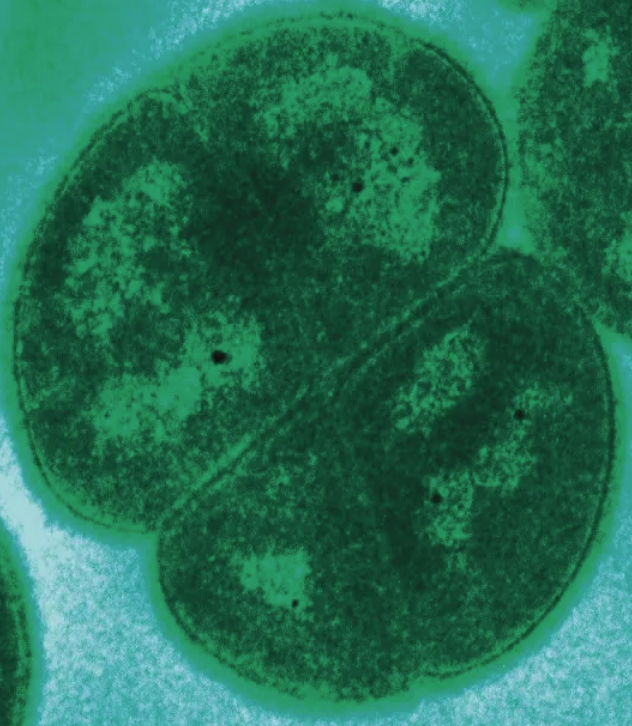
Deinococcus radiodurans — грамположительный, экстремофильный кокк рода Deinococcus, один из самых устойчивых к действию ионизирующего излучения. «Википедия»
— Сторонники панспермии давно говорят про микробы, живущие в межзвездной среде, в составе астероидов, метеоритов, пылевых облаков. Но, насколько мне известно, условия в этой среде все-таки слишком жесткие — и по низкой температуре, и по радиации, — чтобы микробы с медленным метаболизмом — а быстрого там из-за температуры не будет — могли это пережить. Да, существуют устойчивые к радиации микробы, такие как Deinococcus radiodurans, но устойчивость у них обеспечивается только за счет очень быстрого обмена веществ, быстрой репарации ДНК и быстрого роста. В покоящемся состоянии их устойчивость сильно снижается. То есть сочетание радиации и холода в межзвездной среде мне кажется очень неблагоприятным для всех известных микробов. Мне сложно представить себе активно развивающуюся жизнь в межзвездной среде на метеоритах и на пылинках. То есть мертвые, выброшенные с планет следы жизни мы там встретить можем, а вот натолкнуться на жизнь, для которой это родная среда — уже маловероятно…
— Тут можно привести в качестве аргумента какие-то простые организмы, причем животных, например нематоды, которых живьем находят через десятки тысяч лет в мерзлоте. Они как-то репарируют ДНК, а ведь за сто тысяч лет они получают очень приличную дозу радиации.
— Они не репарируют ДНК в вечной мерзлоте, но уровень радиации, который они встречают в подобной среде на Земле, значительно ниже, чем в среде межзвездной, за пределами магнитосферы Земли и Солнца.
— Он ниже на два порядка — даже не на два, а чуть меньше, чем на два. Но, наверное, можно себе представить какую-нибудь тварь, которая как-то может к этому приспособиться. Я-то как раз в это не верю, но что тут надо ответить возможным оппонентам?
— Я не готов обещать съесть собственную шляпу, если межзвездные микробы все-таки будут обнаружены, но мне кажется, что это маловероятно, на грани возможного. Такую возможность я немножко допускаю.
— Ну да, мне тоже так кажется, но опять же это спекуляции. На этом давайте закончим. Михаил, большое спасибо вам и всем зрителям, которые дослушали интервью до конца. До свидания!
— До свидания.

